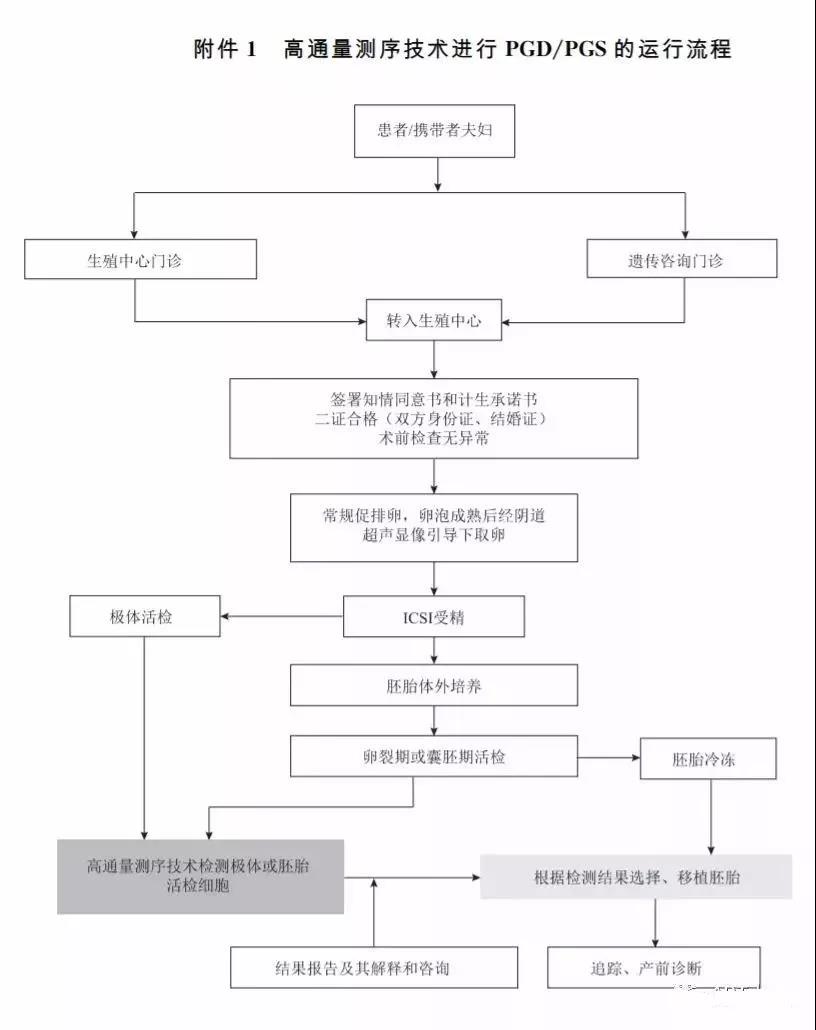
根據國家衛生和計劃生育委員會發布的《關于輔助生殖機構開展高通量基因測序植入前胚胎遺傳學診斷臨床應用試點工作的通知》要求,特制定《高通量基因測序植入前胚胎遺傳學診斷技術規范(試行)》(以下簡稱“本規范”)。本規范針對“高通量基因測序技術在人類胚胎植入前遺傳學診斷(pre-im-plantation genetic diagnosis,PGD)和植入前遺傳學篩查(pre-implantation genetic screening,PGS)的臨床應用”(以下簡稱“本項技術”),明確開展本項技術的基本條件、組織管理、臨床流程與質量控制等方面的基本要求。在人類PGD/PGS的臨床應用中采用高通量基因測序技術(以下稱本項檢測)的機構須遵守本規范。
壹
基本條件
一、機構設置條件
1.本項技術須在醫療機構實施;
2.該醫療機構必須是經省級醫療行政管理部門批準正式并規范運行體外受精-胚胎移植技術、卵胞漿內單精子注射技術和植入前遺傳學診斷技術且是實施本項技術的試點或正式運行單位(以下簡稱“機構”);
3.機構須具有省級臨床檢驗行政管理部門審批核發的臨床基因擴增檢驗實驗室資質,相關工作開展符合《臨床基因擴增檢驗實驗室工作規范》的規定。
二、設備條件
機構須具備細胞遺傳學實驗診斷的設備和上述第一部分第一條第3款所要求的相應設備。在此基礎上,機構應同時具備專業的高通量測序技術相應的核心設備(如與第三方合作可由第三方提供),該設備由經衛生行政管理部門批準試點或正式開展高通量測序技術臨床應用的單位生產。各種設備的種類、數量須與實際開展的項目及工作規模相匹配。
三、人員條件
1.實施本項技術的醫療機構必須建立與本項檢測工作相適應的專業技術人員團隊。其中包括:具備從事產前診斷技術資質的副高職稱以上的臨床醫師2名以上(含2名,下同);具備臨床檢驗資質的中級職稱以上的實驗室技術人員1名以上;具備醫學、生物學或遺傳學本科及以上學歷的專業技術人員3名以上;
2.實施本項檢測工作的專業技術人員必須具有臨床基因擴增檢驗實驗室技術人員上崗培訓合格證;
3.實施本項技術的專業技術人員中2人(其中1人可來自第三方合作機構)以上必須具備專業的生物信息學、檢測結果分析與判讀的知識和能力。
四、場所條件
1.具有符合PCR診斷實驗室標準的PGD專用的實驗場所,包括樣品處理區、試劑配制區、全基因組擴增區、文庫構建及檢測區、測序區和產物分析區等;通過了省臨檢中心的審查,獲得“臨床基因擴增檢驗實驗室技術驗收合格證書(PCR證書)”;
2.胚胎活檢場地布局合理,符合輔助生殖技術胚胎培養室的潔凈要求;
3.工作場所須符合醫院建筑安全要求和消防要求,保障水電供應。各工作場所應具備必要的消毒和空氣清潔設施。
貳
組織管理
一、高通量測序PGD/PGS的組織管理
1.實施本項技術的醫療機構及其人員,必須遵守國家人口和計劃生育法規和條例的規定,并與患者簽署《高通量測序技術進行PGD/PGS知情同意書》和《高通量測序技術進行PGD/PGS妊娠后隨訪和接受產前診斷知情同意書》;
2.機構必須預先認真查驗接受本項技術的夫婦的身份證、結婚證,備案其紙質復印件,并取得接受本項技術的夫婦對于遵守國家人口和計劃生育法規和條例規定的書面承諾的原件;涉外婚姻夫婦及外籍人員應出示護照及婚姻證明并備案其紙質復印件;
3.機構必須制定并嚴格實施避免非醫學指征性別診斷的措施,杜絕非醫學指征的性別鑒定。除性染色體存在有病理意義異常的病例,本項檢測報告發布時必須隱去性別的檢測結果。機構必須制定詳細、可操作的在可用胚胎中選擇移植胚胎的標準及其操作程序。選擇移植胚胎的結論須由除遺傳檢測相關人員以外的臨床正高職稱一名和胚胎培養室副高職稱以上的一名專業人員共同簽署相同的意見。移植胚胎妊娠分娩或失敗后憑相關資料及中心負責人簽署的意見追溯所移植胚胎的性別診斷結果并在病案和數據庫中記錄;
4.機構可根據自身條件獨立開展本項檢測,也可擇優與經衛生行政管理部門批準的高通量測序技術臨床應用于胚胎植入前遺傳學診斷的試點或正式運行的醫學檢驗機構簽訂合作進行本項檢測的服務協議,將測序交由對方進行。
(1)獨立開展本項檢測的機構,必須采取必要措施保證本項技術的質量并定期進行評價,按本規范開展工作。
(2)與上述合作醫學檢驗機構在本機構內共建聯合實驗室或交由上述合作方進行本項檢測的醫療機構,由雙方合作開展本項技術。醫療機構與合作方須簽訂合作協議,明確雙方權責:
①對外合作的醫療機構必須是符合本規范第一部分基本要求所規定的醫療機構;
②醫療機構負責臨床醫療行為,包括病例的篩選、PGD/PGS方案的確定、檢測前的咨詢、簽署知情同意書、樣本采集、報告簽署和發放、結果解釋、臨床處理、質量評價、醫療風險管理等;
③與醫療機構合作的醫學檢測機構負責提供有效的檢測技術,包括檢測技術平臺的建設、技術人員的培訓、技術支持、檢測的質量控制、提供檢測結果及其解釋等;
④醫療機構負有對合作的檢驗機構的資質、場所、設備、人員、技術等條件和檢測能力進一步核實的責任,合作的檢驗機構須無條件提供有關材料并配合該項核實工作。合作的檢驗機構須建立有效可行的措施保障本項檢測的質量;雙方應定期對此進行評價,并按本規范開展工作。
5.如衛生行政管理部門指定機構進行本檢測技術的實驗室間比對等質量控制工作,各機構須予以全面配合,其質控結果應定期上報衛生行政主管部門指定的相關部門或機構。
二、定期報告
實施本項技術的醫療機構必須定期進行自查,定期將實施本項技術的工作量及其結果和各項技術指標包括高通量測序的檢出率、陽性率、陰性率和誤診率等數據上報衛生行政管理部門指定的相關部門或機構。
三、定期評估
機構必須接受衛生行政管理部門組織的專家組對本項技術實施的指導、監督和對各機構的質量控制、場所、設備、試劑、人員、技術、檢測方案、檢測效果、管理制度的執行等事項的定期評估,執行根據評估情況提出的調整或改進的建議,以及暫停、終止機構實施本項技術的意見。
叁
高通量測序技術PGD/PGS的臨床流程
一、適應證和禁忌證
1.適應證:(1)高通量測序PGD的適應證:包括多種遺傳疾病如基因性疾病、非平衡的染色體結構異常、染色體數目異常,以及染色體微小片段插入、缺失與重復等;(2)高通量測序PGS的適應證:自然流產≥3次、或2次自然流產且其中至少1次流產物檢查證實存在病理意義的染色體或基因異常的患者,反復種植失敗(移植優質胚胎3次及以上,或移植不少于10個可移植胚胎)的患者,也可用于>38歲的高齡且需要采用輔助生殖技術的患者。
2.禁忌證:有如下情況之一者,不得實施PGD技術:
(1)患有《母嬰保健法》規定的不宜生育的遺傳性疾病;
(2)患有目前無法進行胚胎植入前遺傳學診斷的遺傳性疾病;
(3)其它不適宜實施輔助生殖技術的情況。
二、工作程序
對具備適應證的患者,醫師應在其夫婦雙方簽署知情同意書后,予以核查并備案相關證件,進行術前檢查并排除禁忌證;建立病歷檔案;按輔助生殖技術程序促排卵后經陰道穿刺取卵,行卵胞漿內單精子注射授精,胚胎體外培養,擇時行胚胎活檢,獲取樣本進行高通量測序、生物信息學分析,確定胚胎的相關遺傳性狀是否適合進行胚胎移植,適時向接受本項技術的夫婦雙方報告并解釋胚胎的高通量測序檢測結果,選擇胚胎進行宮腔內移植;成功妊娠后須跟蹤患者妊娠情況,擇時進行產前診斷,根據產前診斷結果作相應處理,并隨訪妊娠最終結局和子代情況。具體流程可參考附件1制定。