自新冠疫情爆發以來,已對全球造成了巨大的健康威脅。但是,目前為止尚未找到有效的治療方法,因此,全球無數科學家都在努力測試相關藥物和研發相關疫苗。

2020年5月7日,劉磊、高福和高峰等研究團隊曾在預印本平臺發表題為“A non-competing pair of human neutralizing antibodies block COVID-19 virus binding to its receptor ACE2”的文章,該研究從一名新冠肺炎康復患者體內分離了兩種具有不同抗原表位的單克隆抗體——B38和H4,并通過細胞實驗和小鼠實驗表明這兩種單抗可以有效阻斷新冠病毒與其受體ACE2的結合,并且有助于COVID-19患者的治療和相關疫苗的開發。

2020年5月26日,Nature更是同期刊發兩篇中國團隊的文章,兩篇文章均表示純化到了潛在的人源SARS-CoV-2中和抗體。其中高福與嚴景華、王奇慧、袁志明、王福生等領導的研究團隊發表了題為“A human neutralizing antibody targets the receptor binding site of SARS-CoV-2”的文章,該文報道從一名新冠肺炎康復期患者體內分離到2個特異性人源性單克隆抗體(McAb)。CA1和CB6具有較強的SARS-CoV2特異性體外中和活性。此外,CB6在預防和治療兩方面都能抑制恒河猴的SARS-CoV-2感染,這表明CB6值得進一步臨床轉化。

2020年6月6日,由高福與中國食品藥品檢定研究院李長貴、清華大學婁智勇、沈陽藥科大學徐苗、中國醫學科學院秦川、疾控中心武桂珍、譚文杰、國家聯合疫苗工程技術研究中心楊曉明等多個團隊聯合在Cell發表了題為“Development of an inactivated vaccine candidate, BBIBP-CorV, with potent protection against SARS-CoV-2”的文章。
該文報道了研究人員對一種SARS-CoV-2滅活疫苗(BBIBP-CorV)進行了中試生產,并表示該疫苗能在小鼠、大鼠、豚鼠、兔子和非人靈長類動物(食蟹猴和獼猴)中誘導高水平高效價的中和抗體,以提供對SARS-CoV-2的免疫。使用2個劑量(2μg/劑量)的BBIBP-CorV進行免疫,即可讓恒河猴免于通過氣管感染SARS-CoV-2,并且沒有檢測到抗體依賴性感染增強。此外,BBIBP-CorV在疫苗生產中表現出高效的生產效率和良好的遺傳穩定性。這些結果表明,BBIBP-CorV值得進行進一步臨床評估。
首先,研究人員從3名住院患者的支氣管肺泡灌洗液或咽拭子中分離出了3株SARS-CoV-2毒株:19nCoV-CDC-T an-HB02 (HB02)、19nCoV-CDC-T an-Strain03 (CQ01) 和19nCoV-CDC-T an-Strain04 (QD01)。經過一系列測試,發現HB02這一病毒株最適合進一步研究,并使用該毒株制備了相關滅活疫苗。
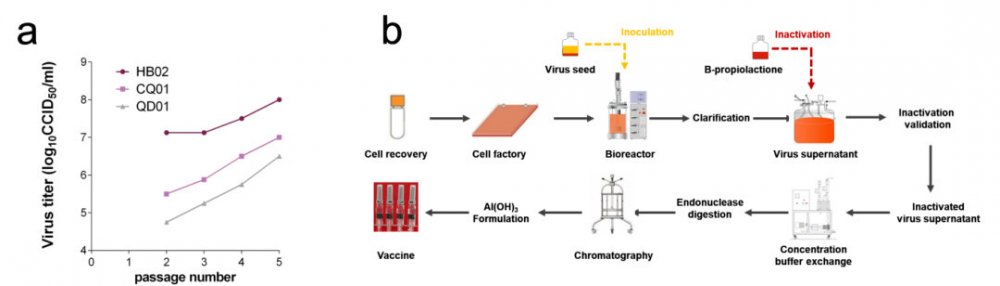
接下來,研究人員測試了利用該毒株制備的疫苗在不同動物(大鼠、小鼠、豚鼠、兔子、食蟹猴)體內的免疫情況。分別測試了一次性免疫和兩次免疫的情況,結果發現,在高、中、低劑量(8、4、2μg/dose)的免疫情況下,兩次免疫均要好于一次性免疫。
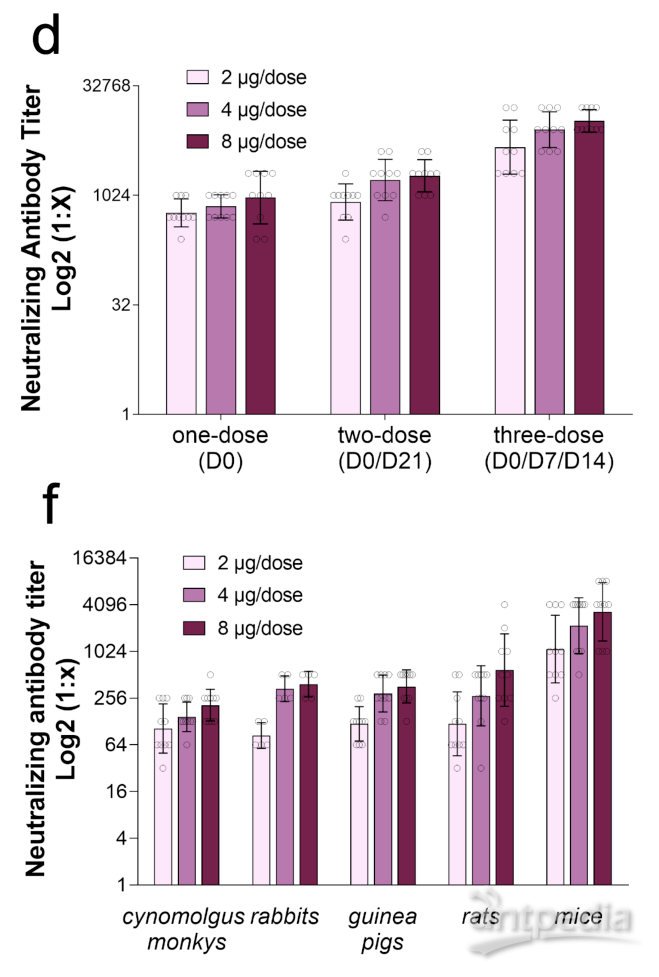
最近研究表明,恒河猴感染SARS-CoV-2會出現與人類類似的肺部浸潤和組織損傷,所以作者又在恒河猴身上對該疫苗進行了相關測試。結果發現,BBIBP-corv低劑量和高劑量均能有效地保護恒河猴抵抗SARS-CoV-2,而且沒有觀察到抗體依賴性的感染增強作用。
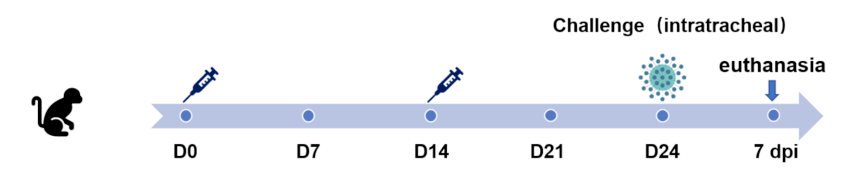
總之,該文結果表明,BBIBP-CroV疫苗是一個針對COVID-19的潛在高效安全的疫苗,并且作者表示,研究人員已經基于本文的結果正開展I期臨床試驗,II期臨床試驗也已經于近期啟動,在該臨床試驗中主要是測試高、中、低三個劑量組的免疫情況,從而確定后期臨床應用的合適劑量。
為深化區域聯動、共筑監管合力,更好地貫徹國家藥監局著力提升藥物臨床試驗監管能力、著力提升藥物臨床試驗研究能力、持續加強臨床試驗監管的要求,6月11日至13日,寧夏回族自治區藥品監督管理局聯合甘肅省、青......
國家藥監局關于發布免于進行臨床試驗體外診斷試劑目錄(2025年)的通告(2025年第23號)根據《體外診斷試劑注冊與備案管理辦法》(國家市場監督管理總局令第48號),國家藥監局組織修訂了《免于進行臨床......
6月16日,國家藥監局綜合司發布《關于優化創新藥臨床試驗審評審批有關事項的公告(征求意見稿)》(以下簡稱“《征求意見稿》”),推出創新藥臨床試驗“30日快速審批通道”,旨在進一步支持以臨床價值為導向的......
國家藥監局藥審中心關于發布《阿爾茨海默病藥物臨床試驗技術指導原則(試行)》的通告(2025年第19號) 為指導阿爾茨海默病藥物的科學研發和評價,提供可供參......
關于公開征求《老年人群參與創新藥臨床試驗的關鍵要素及試驗設計要點(征求意見稿)》意見的通知 為更好地落實ICHE7指南要求,推動我國創新藥研發中老年人群臨......
近日,國家藥監局印發《關于發布醫療器械臨床試驗項目檢查要點及判定原則的公告》(2025年第22號,以下簡稱《公告》)。現就《公告》相關內容說明如下:一、《公告》修訂背景為進一步加強醫療器械臨床試驗監督......
國家藥監局關于發布醫療器械臨床試驗項目檢查要點及判定原則的公告(2025年第22號)為規范醫療器械臨床試驗檢查工作,統一檢查范圍和判定標準,提高醫療器械臨床試驗項目檢查質量,根據《醫療器械監督管理條例......
1月9日,美國眾議院“中國特別委員會”(以下簡稱委員會)多名議員發給商務部長GinaRaimondo的一封公開信顯示(以下簡稱公開信),建議對計劃在中國軍方相關設施開展合作或試驗的企業實施更嚴格的出口......
國家藥監局藥審中心關于發布《藥物臨床試驗樣本量估計指導原則(試行)》的通告(2024年第54號)為指導申辦者在藥物臨床研發過程中進行科學合理的樣本量估計,藥審中心組織制定了《藥物臨床試驗樣本量估計指導......
12月13日,在北京市科學技術委員會和中關村科技園區管理委員會的支持下,細胞出版社與清華大學醫學院在清華校園聯合舉辦了2024中關村論壇系列活動暨北京國際學術交流季——從實驗室到臨床:細胞與基因治療的......