德國 KNAUER 碰撞噴射混合器(IJM)
BioNTech/Pfizer COVID-19 疫苗所有生產工廠均采用本套設備。
更多詳細資料請聯系:劉先生 15201316651(微信同號)
新冠疫情的持續凸顯了疫苗的重要性以及全球對疫苗的迫切需求。借此契機,mRNA疫苗登上了舞臺,并以極高的保護率成為所有新冠疫苗種類中熱度最高的C位選擇。本報告介紹分析了mRNA疫苗相較于其他技術路徑疫苗的優勢,mRNA疫苗的核心技術,以及未來的發展空間和方向。
前言
mRNA疫苗:疫苗行業新王朝的崛起
免疫系統及疫苗工作原理
免疫系統概覽
獲得性免疫作用原理
疫苗一般性原理
mRNA疫苗
mRNA疫苗相較于其他技術路徑疫苗的優劣勢分析
mRNA新冠疫苗臨床數據解析:No pain, no gain
mRNA疫苗展現了令人振奮的保護率
mRNA疫苗不良反應:短期反應略高于傳統疫苗,需要時間驗證長期安全性
mRNA疫苗臨床數據特點:No pain,No gain
mRNA疫苗嚴重/致命性不良反應罕見但需關注
新冠疫情為mRNA疫苗登上舞臺帶來機遇
mRNA疫苗效果初顯,免疫屏障減緩病例新增
短期:國產mRNA疫苗應聚焦海外放量
中長期:病毒變異或削弱一代疫苗效力,mRNA疫苗可快速反應應對變異
mRNA疫苗生產流程
第一步:DNA質粒制備
第二步:體外轉錄
第三步:遞送系統裝載
第四步:灌裝檢驗
mRNA疫苗兩大核心競爭力:序列結構、遞送系統
mRNA序列結構決定抗原蛋白結構、免疫原性及穩定性
遞送系統是目前產能擴張的瓶頸
mRNA疫苗有望為腫瘤免疫疾病控制帶來新曙光
mRNA疫苗屬性契合腫瘤免疫疾病控制需求
mRNA疫苗能夠激發針對細胞的T細胞免疫
mRNA疫苗能夠更精準地靶向特異免疫目標
mRNA腫瘤疫苗研發情況
輝瑞mRNA疫苗CNN報道
mRNA疫苗:疫苗行業新王朝的崛起
2020年初,一場突如起來的傳染病大流行給全世界帶來了巨大變數。擁有與18年前“非典”罪魁禍首SARS病毒相似的部分結構,新型冠狀病毒(SARS-CoV-2)甚至擁有了更強大的傳染能力和應對溫度變化的能力。全球每月新增病例數一路走高,春夏秋冬的自然變化對病毒幾乎無影響。在此情況下,人類把終結這一疫情大流行的唯一希望寄托在疫苗的出世。各國醫療機構、企業紛紛投入這一領域中。新冠疫苗研發既讓企業履行了社會責任,同時也給予企業巨大的市場空間。全球總人口超過77億,建立起全球性的免疫屏障需要百億劑以上的新冠疫苗。在此雙重激勵下,全球涌現出許多優秀的疫苗企業,以中美德三國為領導者,在1年內用前所未有的速度研制出相應的新冠疫苗,讓深陷疫情泥潭的世界看到了曙光。而這些優秀的疫苗中,剛剛登上舞臺便最為閃耀的一個品種是mRNA疫苗。
mRNA疫苗打破了傳統滅活、減毒疫苗的免疫激活模式,創新性地利用人體本身細胞生產抗原,以此激活特異免疫。mRNA疫苗具有極高的有效保護率,同時相較于其他創新型疫苗(如:DNA疫苗、病毒載體疫苗)具有更高的安全性。在研發上,mRNA疫苗能夠快速地更新迭代以應對不斷出現的變異毒株。由于mRNA疫苗不需進行體外轉譯,因此生產過程也有所縮短,僅需要60-70天。
美國疫情的好轉印證了mRNA疫苗的有效性。自美國總統拜登簽署“百日疫苗接種計劃”后,美國每日新增病例顯著下降。
國內第一輪疫苗接種已接近尾聲,短期內疫苗需求落至低點,但海外疫情持續蔓延,市場機會可觀。長期來看,隨著滅活疫苗有效期臨近以及病毒變異加速,在2021年底2022年初國內可能會出現第二輪疫苗需求的高峰。
mRNA的應用前景非常廣闊。除了能夠用于預防傳染性疾病,mRNA疫苗也為治療腫瘤、免疫疾病帶來了新的星火。在新冠疫情前,國際mRNA廠商的研究重點集中在腫瘤的治療上。目前國際mRNA疫苗三巨頭為:BioNTech、CureVac、Moderna,均布局了多條針對腫瘤的管線。除傳染病和腫瘤免疫疾病外,mRNA疫苗在許多基因相關的疾病中都有開發潛能。在后新冠疫情時代,mRNA疫苗仍舊具備大幅增長的潛力。
mRNA疫苗的技術壁壘在于序列設計和遞送系統。序列設計需要公司擁有大量長期的數據積累,不斷訓練優化平臺。優秀的序列設計能夠提高mRNA在體內的留存和作用時間,降低免疫原性,使mRNA序列更高效地表達抗原蛋白。遞送系統則是mRNA的運載火箭,負責將mRNA成分完整地運送至目標靶點,并且在合適的時機和環境條件下及時釋放。同時,遞送載體需要經過人體免疫系統的層層保護,容易引起過敏等免疫反應,傷害疫苗的安全性。遞送系統還很大程度決定了mRNA疫苗的儲藏條件和儲藏時限。目前擁有此技術的公司非常稀少,同時具有ZL保護壁壘,是mRNA疫苗行業“卡脖子”的技術之一。
艾博生物、斯微生物是國產mRNA疫苗進展最快的兩家企業,除此之外,復星醫藥獲得了BioNTech新冠疫苗大中華區的代理,mRNA新冠疫苗能否為公司創造盈利值得持續關注。
免疫系統概覽
人體免疫系統是一個以功能作為定義的系統,而非由器官作為定義的系統。其中包含皮膚、黏膜等物理屏障,肝臟等器官分泌的蛋白化學物質,也包括巨噬細胞、T細胞等生物類保護分子。
免疫系統可分為固有性和獲得性免疫。
固有性免疫是人體天生帶有的免疫系統,具有非特異性、反應快速等特點。獲得性免疫則具有特異性,在首次感染時反應較慢。
一般情況下,抵御外源性入侵物質的第一道防線是固有性免疫。固有免疫中又可分為外部防御和內部防御。外部防御的典型是皮膚以及黏膜,是人體整套防御系統的排頭兵。若外部防御被突破,內部防御將筑起第二道防線,其中包括吞噬細胞、抗微生物蛋白質、自然殺手細胞(NKcell)等。
若固有免疫無法成功防御入侵,獲得性免疫則會啟動。由于獲得性免疫具有特異性,因此針對特定入侵物質的防御效果較為明顯。常見的獲得性免疫可分為體液免疫和細胞免疫。目前,幾乎所有疫苗的最終目的都是激活此處所提到的獲得性免疫。
獲得性免疫作用原理
如其名,獲得性免疫指后天得到的免疫。具體可分為體液免疫和細胞免疫。
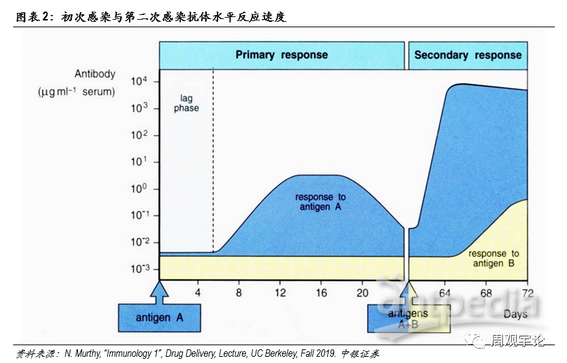
體液免疫的核心細胞是B細胞(B cell)。原始B細胞在接觸到外源性抗原后便被激活,并根據抗原成長分化為特異性B細胞,開始分泌特異性抗體。抗體能夠識別入侵病原體表面的抗原,并與其結合。抗體本身沒有殺死病原體的物質,但它能夠與病原體結合使其失去感染其他細胞的能力,同時引導其他免疫細胞,例如巨噬細胞,將病原體吞噬,一些抗體能加速病原體細胞的分解。根據克隆選擇理論(thecolonal selection theory),病原體被殺滅后,特異化B細胞會繼續留在體內,成為免疫系統的一段“記憶”。若再次遇到相同抗原時,留存的B細胞便能快速擴增、分泌抗體,而不需重新從原始B細胞開始分化。因此,首次感染時,B細胞特異免疫反應較慢;而后二次感染時,B細胞特異免疫反應速度則非常迅速。同時,由于特異性B細胞會留存于體內,抗原出現頻率越頻繁,針對此抗原的特異性B細胞擴增數量越多,因此,特異免疫的反應也會越來越快越來越強。這是許多疫苗需要多劑次加強的原因。
細胞主導免疫的核心細胞是T細胞(T cell)。T細胞分為2類:輔助T細胞(CD4+)和殺手T細胞(CD8+)。當外源性蛋白質進入體內,部分蛋白會被抗原呈遞細胞(Antigen Presenbting Cell,APC)捕捉。常見的APC包括樹突細胞(DendriticCell,DC)、B細胞等。APC通過TLR(Toll-Like Receptor)分辨是否是外來抗原。若識別結果為外來抗原,APC會將抗原片段以抗原-MHC結合體的形式暴露在APC細胞膜表面。當輔助T細胞的受體(TCR)與MHC-抗原結合時,輔助T細胞會開始復制并釋放細胞素,激活B細胞和殺手T細胞。殺手T細胞被激活后通過MHC結構與APC結合,并釋放穿孔素和顆粒酶。穿孔素會附著在目標細胞膜上形成穿孔,顆粒酶通過穿孔進入細胞內部溶解細胞。當病原體消滅后,部分CD4+和CD8+T細胞會繼續留在體內,稱為記憶T細胞。與記憶B細胞類似,記憶T細胞擁有對抗原的特異性。若未來遭遇相同的外來抗原,T細胞能夠迅速擴增激活,殺滅入侵的病原體。
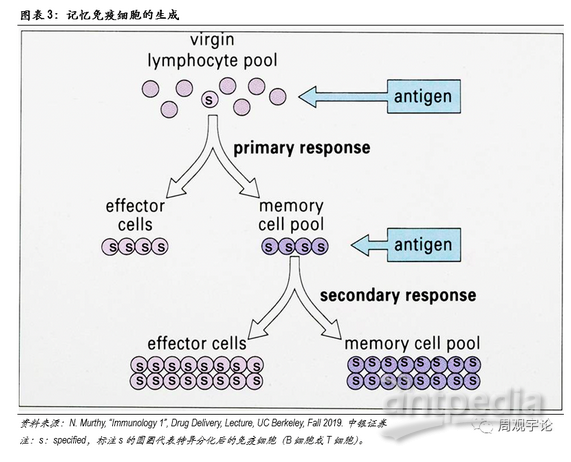
總體而言,獲得性免疫的激發來源于對抗原的識別。當某一病原體首次入侵時時,由于沒有現成的特異化B細胞和T細胞,獲得性免疫的應答時間較長。原始B細胞和T細胞需要時間分化形成特異性免疫細胞。在完成首次殺滅后,部分特異化的B細胞和T細胞會留存于體內成為記憶B細胞、記憶T細胞。若未來再次遭遇相同抗原入侵,無需原始B/T細胞重新分化,記憶B細胞和T細胞將自我擴增、激活,迅速啟動免疫應答。
疫苗一般性原理
疫苗的目的是讓人體形成特異性的記憶B細胞和記憶T細胞。在免疫記憶形成后,若人體遭到此病原體襲擊,獲得性免疫能夠迅速應答,在病原體大規模感染其他細胞前,將病原體和已被感染的細胞殺滅。
目前,絕大部分疫苗的邏輯是通過遞送抗原,使人體自發形成特異性免疫反應。相較于直接注射抗體或特異性T細胞,人體自發形成的免疫具有更好的持續性,同時免疫原性更低。直接注射的外源性抗體或T細胞本質上也屬于外來物質,在人體內容易遭受免疫系統攻擊。同時,抗體和T細胞本身具有半衰期,免疫有效時間短。由于直接注射的抗體或T細胞無法成為人體免疫記憶的一部分,因此,人體不能直接復制注射進入的抗體或T細胞,所以無法在遭遇抗原時快速擴增,免疫反應較弱。
直接遞送抗體或T細胞的做法不適用于預防領域,但在部分治療領域能夠發揮作用。目前關注度較高的抗體藥便是將人為制造或編輯的抗體導入人體內,直接由注入的抗體對特定細胞進行殺傷或抑制。CAR-T療法則是直接遞送經過人為編輯的T細胞(稱為CAR-T細胞)進入體內,由這部分改裝過的CAR-T細胞直接殺傷目標細胞(例如腫瘤細胞)。
疫苗通過遞送抗原激發人體特異性免疫反應。但與自然界中病原體入侵形成免疫記憶不同,疫苗往往只遞送無毒無害的某一抗原片段進入人體。抗原本身是無害的,可視作一種標識,供免疫細胞進行識別。因此,疫苗本身并不帶有毒性。
mRNA疫苗
mRNA疫苗是一種核酸疫苗,通過將病毒的部分mRNA片段注入人體細胞內產生抗原,再由此激發特異性免疫反應,達到形成免疫記憶的效果。
mRNA疫苗治療原理:“巧”用自身細胞加強特異性免疫
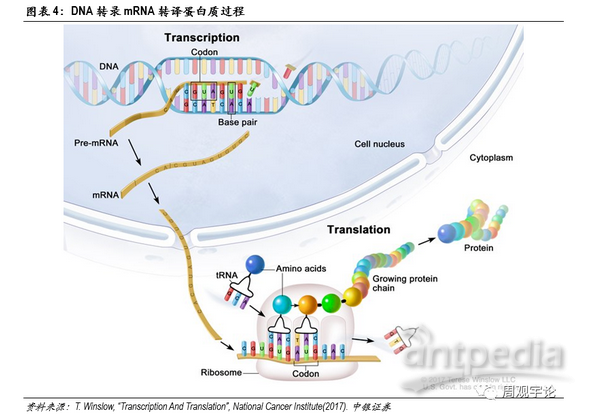
DNA是存儲人體遺傳信息的載體。人體內絕大部分細胞都帶有DNA。但是DNA本身無法直接對人體產生影響,各類蛋白質才是能夠左右表象的物質(例如:抗原、激素)。DNA需要轉化為蛋白質才能夠將遺傳信息表達出來。整個DNA轉化為蛋白質的過程分為兩大步,第一步:DNA轉化為mRNA,這一步驟稱為轉錄(transcription),發生在細胞核內;第二步:mRNA轉化為蛋白質,這一步驟稱為轉譯(translation),發生在細胞質中。可以看到,mRNA是DNA轉化為蛋白質的中間體,這也是它名稱的由來,即信使RNA(messenger RNA)。通俗來講,DNA類似于底稿,DNA發生的改變會一直存在于體內,由此細胞分裂新產生的細胞也會繼承這些改變,因此DNA的改變有很大概率會伴隨一生,其中性細胞中DNA的變化甚至能夠遺傳至下一代。mRNA類似于說明書,能夠指導自身細胞生產出特定的蛋白,但是mRNA的改變不會被分裂產生的新細胞繼承,也不會遺傳至下一代個體中。蛋白則是最終生產得到的工具,對生物個體的各項指標直接產生作用。同樣地,蛋白不會被繼承或遺傳。這一條轉錄轉譯鏈被稱為生物學“中心法則”。mRNA疫苗利用了兩步表達的機理,使疫苗在不改變DNA序列的同時,為人體免疫系統的激活提供更準確的抗原蛋白以及更持久的抗原體內留存時間,使被激活的特異性免疫更精準,同時免疫效果得到鞏固。
具體來分析mRNA新冠疫苗的機理。mRNA疫苗中的mRNA片段編碼新冠病毒表面的某些蛋白或受體,例如刺突蛋白(S蛋白)。疫苗遞送人工編輯后的mRNA進入人體細胞,在體內“借用”人體自身細胞轉譯mRNA為蛋白質。此類mRNA在經過轉譯后會表達成為病毒所具有的某種抗原蛋白。雖然產生的抗原是由自身細胞制造,但由于其氨基酸序列具有外源性,APC中的TLR并不識別此段序列,因此仍舊會激發B細胞和T細胞針對此抗原蛋白的特異性免疫反應,并建立免疫記憶。
LNP遞送系統:遞送疫苗有效物質進入預定軌道的運載火箭
如今,病毒遺傳信息序列的解碼和反向序列合成已不是難題。如何將合成好的mRNA序列遞送進入人體細胞變成了mRNA疫苗研發的重要挑戰之一。
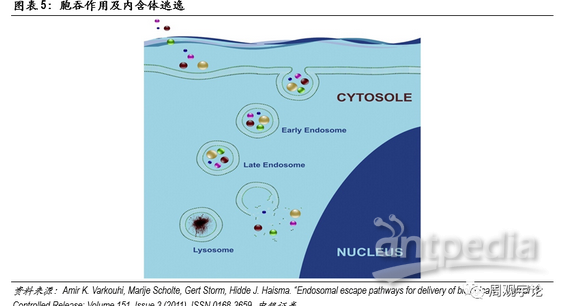
人體細胞結構從外至內可分為細胞膜(cellmembrane)、細胞質(cytoplasm)、細胞核(nucleus)。mRNA轉譯成蛋白質的過程發生在細胞質中,因此,mRNA疫苗要發揮作用,必須先將編輯好的mRNA轉遞進細胞質中。進入細胞質需要通過細胞膜,細胞膜由磷脂雙分子層構成,磷脂分子頭部具有親水性,尾部具有疏水性,兩層磷脂尾部相對形成雙分子層,能夠有效控制水分子、離子、大分子物質通過。mRNA作為大分子(300-5000kDa),在不破壞細胞膜的前提下,進出細胞只能以內含體(endosome)通過胞吞作用(endocytosis)。通常情況下,內含體進入細胞質后,會被直接送至溶酶體(lysosome)進行分解。為保證mRNA在轉譯前保持完整性,mRNA需要在內含體與溶酶體結合前打破內含體包膜(endosomaldisruption)并逃離。逃離內含體進入細胞質后,mRNA便會在細胞質內游動,直至到達核糖體(ribosome)并在此轉譯為肽鏈,最終折疊成為蛋白質。
對于mRNA疫苗和藥物,遞送系統有兩大職責:一是有效包裹和保護mRNA在到達靶點前維持穩定,二是幫助mRNA有效成分進入細胞,三是在mRNA到達溶酶體前將其釋放進入細胞質中。
LNP是目前最具潛力的遞送載體之一。LNP(Lipid Nanoparticle)是脂質微粒的總稱,其中又包括脂質膠團(micelle)、脂質體(liposome)等。LNP與細胞膜的組成成分相似,均由脂質分子構成。脂質分子的兩條長尾通常呈平行狀態,在此狀態下,脂質形成的雙分子層穩定。在進入細胞質酸性環境后,部分脂質的頭部質子化,呈現陽離子形態,與其他陰性離子態的脂質分子相吸引,尾部張開。原本雙分子層的形式被破壞,形成頭部聚集在一起的環狀。之前包裹在內的mRNA便可逃逸出內含體,進入細胞質等待轉譯。
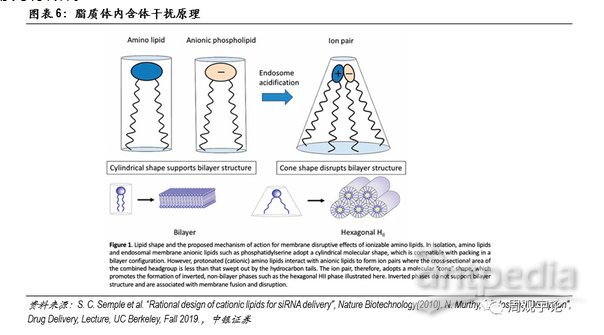
為了提高載體對包裹成分的保護能力,通過在載體外部連接PEG可以進一步增強載體的穩定性。
mRNA疫苗相較于其他技術路徑疫苗的優劣勢分析
(1)mRNA疫苗 vs. 滅活疫苗:具有明顯的免疫保護力優勢
與傳統滅活疫苗、裂解疫苗相比,mRNA疫苗激活特異免疫的路徑不相同。傳統疫苗激活特異性免疫的方式是直接將抗原蛋白注射進入人體,引起免疫反應;而mRNA是將編碼病毒抗原的mRNA注入體內,由人體自身細胞產生對應的抗原,以此激活特異性免疫。理論分析,mRNA疫苗能夠呈現更多的抗原,同時能更持久地激活鞏固特異性免疫。原因在于,傳統滅活疫苗的抗原呈遞數量是一定的,即最終到達體內引起免疫反應的抗原數量只能夠小于或等于疫苗中含有的抗原數量。同時,滅活疫苗呈遞抗原的過程是一次性的,注射時疫苗呈遞的抗原即為所有抗原,這些抗原的降解時長即為持續激活免疫的時長,此后不會有新增抗原。而mRNA疫苗抗原呈遞的過程是可短暫持續的,呈遞的mRNA可指導多個核糖體產生抗原蛋白,直至mRNA 降解。由于細胞能夠不斷根據mRNA生產抗原蛋白,因此抗原數量受疫苗劑量所限制較小,從時間維度上看,抗原不會在短時間內迅速被消耗完畢。抗原數量水平越高、保持時長越長,形成的特異性免疫記憶越強烈,免疫應答更快、持續時間越長。
(2)mRNA疫苗 vs. DNA疫苗:更高效,逆轉錄風險較小
與核酸疫苗中另一路徑的DNA疫苗相比,mRNA疫苗更有效也更安全。DNA疫苗需要將包裹的有效成分遞送通過兩層屏障:細胞膜和細胞核膜,最終進入細胞核內開始抗原蛋白的表達。多層屏障導致有效成分難以進入反應場所,免疫激活更難。同時,由于DNA疫苗呈遞的有效成分需要進入細胞核內,導致外源遺傳片段逆轉錄進入人體DNA的概率增加,引起腫瘤癌癥的概率增加。相較而言,由于mRNA疫苗導入的外源物質不需進入細胞核,發生外源遺傳片段逆轉錄進入人體自身DNA的概率較小,因此引起腫瘤癌癥的概率極小。
(3)mRNA疫苗 vs. 病毒載體疫苗:適用人群覆蓋全面,逆轉錄風險較小,機會成本更低
LNP為遞送mRNA片段到達靶點、定點釋放提供了支持。另一大受到較高關注度的載體平臺是病毒載體平臺,常見的類別有腺病毒(Adenovirus)、腺相關病毒(Adeno-Associated Virus,AAV)、慢病毒(lentivirus)。病毒載體通過去除病毒本身的有害物質,保留感染能力,將目標物質遞送進入細胞內,由細胞產生抗原蛋白,進而引起特異性免疫反應。病毒載體反應的一大缺陷是,若接種者本身體內含有針對此病毒載體的抗體(如腺病毒、AAV、慢病毒,而非針對目標抗原的抗體),或在短時間內快速產生了抗體,則病毒載體疫苗無法將有效成分遞送進入預定的細胞質內。相比之下,LNP的結構由脂質分子構成,載體引起免疫反應的幾率較小,能夠更有效地遞送有效成分至目標靶點。除此之外,部分病毒平臺有發生逆轉錄的概率,會將外源基因整合進入人體DNA中,可能導致腫瘤、免疫疾病等。同時,病毒載體疫苗具有更高的機會成本。當人體接受病毒載體疫苗注射后,體內會自動產生針對此載體的抗體和其他特異免疫反應。此后再次運用相同或相似病毒載體作為遞送系統給藥時(例如一些腫瘤治療藥物),會更容易遭到免疫系統的攻擊,難以成功將藥物遞送至靶點。
mRNA疫苗的臨床運用歷史始于2020年新冠疫情。根據WHO數據,截止2021年5月7日,全球共有15款mRNA疫苗在研,其中包括已納入WHO緊急使用名單(Emergency Use Listing,EUL)的2款mRNA疫苗:由輝瑞/BioNTech聯合研發的BNT162b2,以及由Moderna研發的mRNA-1273。
mRNA疫苗展現了令人振奮的保護率
2020年11月18日,輝瑞發布了BNT162b2的III期臨床試驗結果,結果顯示疫苗整體保護率高達95%。2021年3月31日,Moderna發布了mRNA-1273的III期臨床試驗結果,結果顯示疫苗整體保護率也達到94.1%,與BNT162b2的數據非常接近。2款mRNA疫苗同時展現出極為優異的保護率,共同預示著mRNA疫苗技術在激活免疫系統上的令人震驚的高效,也讓科學界對mRNA疫苗技術未來在其他疾病領域可能帶來的改變充滿期待。同時,mRNA疫苗在65歲及以上的老年群體中,仍能高效地激發免疫反應,保護率穩定在高水平。
(1)輝瑞/BioNTech mRNA疫苗(BNT162b2)有效性
臨床試驗數據分為兩部分。第一部分,樣本人群為在實驗前或實驗開始時均未感染新冠病毒的人群,本樣本人群共有36523人,其中疫苗組18198人,均接受2劑BNT162b2注射;另外18325人為安慰劑組,接受2劑安慰劑注射。在完成2劑接種7天后,疫苗組出現8例新冠感染者,安慰劑組出現162例,疫苗有效保護率達到95.0%。
第二部分樣本人群包括感染和未感染新冠病毒的人群。樣本人數40137人,其中疫苗組19965人,安慰劑組 18325人。在完成2劑接種7天后,疫苗組中出現9例新冠感染者,安慰劑組169例。疫苗有效保護率達到94.6%。
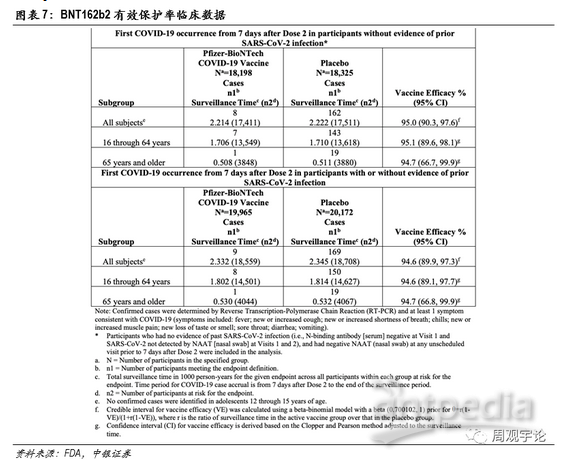
根據年齡段劃分,BNT162b2對16-64歲人群的保護率為95.1%,對65歲及以上的老年群體保護率則維持在了94.7%。數據顯示了mRNA疫苗在人群中激活免疫系統的能力基本不受接種者年齡的影響。
(2)Moderna mRNA疫苗(mRNA-1273)有效性
全球領先上市的另一款mRNA新冠疫苗是Moderna公司與美國國家過敏及傳染疾病研究所(NIAID)研發的mRNA-1273。這款疫苗的技術路徑與輝瑞/BioNTech的mRNA疫苗相同,臨床結果也展現了令人振奮的保護率,以及較低的不良反應發生概率。
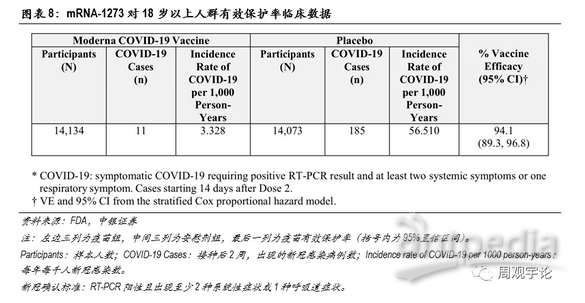
根據Moderna公司給醫療服務機構的事實陳述,mRNA-1273的保護率達到約94.1%(95%CI:89.3%-96.8%)。
在針對18歲以上人群的臨床試驗中,科學家將樣本人群分為兩組:疫苗組14134人,均接受2劑mRNA-1273注射;另外14073人為安慰劑組,接受安慰劑注射。在完成第2劑接種14天后,疫苗組中出現新冠病例11例,每年每千人病例數為3.328;安慰劑對照組中出現新冠病例185例,每年每千人病例數為56.510。由此測得,疫苗保護率約為94.1%,與輝瑞/BioNTech的mRNA新冠疫苗臨床有效率非常相近。Moderna和輝瑞/BioNTech mRNA疫苗的臨床實驗結果都顯示出采用mRNA技術路徑的疫苗具有極高的有效性。
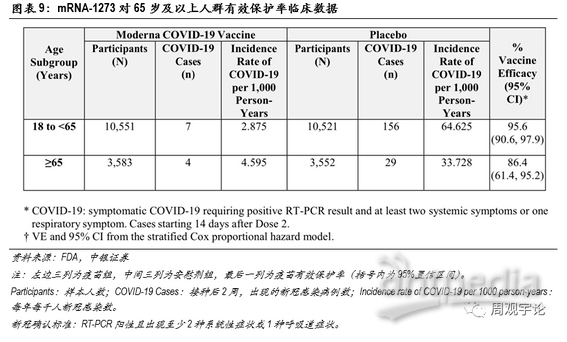
本次臨床試驗的樣本人群中包含了65歲及以上的老年人群,疫苗組中有3583位老年人,其中出現4例新冠感染;安慰劑組中有3552位老年人,其中出現29例新冠感染。因此,mRNA-1273對于65歲及以上的人群的有效保護率為86.4%,表現仍舊非常優秀。
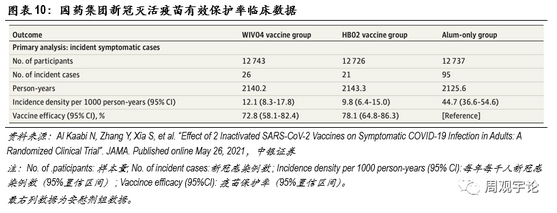
(3)國藥集團滅活疫苗(WIV04/HB02)有效性
為了更直觀地展現mRNA疫苗與傳統疫苗在不同指標上的差別,我們在此引用使用最為廣泛的滅活型疫苗進行對比。國藥集團及北京生物研究所、武漢生物研究所共同研發的WIV04和HB02是2款最先上市的傳統滅活疫苗。
2021年5月26日,JAMA發布了國藥集團2款滅活新冠疫苗的臨床III期結果。臨床結果展現了不錯的保護率,整體保護率均在70%以上,遠遠超出了世界衛生組織50%的要求。
具體數據如下:接種WIV04 的12743人中,出現26例新冠感染;接種HB02的12726人中,出現21例新冠感染;安慰劑組共12737人,出現95例新冠感染。由此可計算得到WIV04的保護率為72.8%(95%CI:58.1-82.4),HB02的保護率為78.1%(95%CI:64.8-86.3)。2款滅活疫苗整體保護率相近,但是與2款mRNA疫苗>90%的保護率相比,仍舊略遜一籌。
mRNA疫苗不良反應:短期反應略高于傳統疫苗,需要時間驗證長期安全性
除了有效保護率外,疫苗的另一重要指標是不良反應發生的種類和概率。總體來說,滅活疫苗因其成熟的技術和研發生產經驗,不良反應發生頻率較低,反應程度也較為溫和。mRNA疫苗則運用了全新的技術,目前得到的安全數據只反映了接種后短期內可能發生的不良反應,是否會對人體造成長期的影響還需要時間進行長期的觀察。
從理論分析,mRNA疫苗通過使部分人體細胞表達外源抗原來激活免疫,除了抗原本身會引起免疫反應,這部分表達抗原的自體細胞可能也會引起較強烈的免疫反應。滅活疫苗則是直接呈遞抗原,因此免疫反應較小。
(1)輝瑞/BioNTech mRNA疫苗(BNT162b2)安全性
臨床試驗記錄了樣本人群每劑次接種后7天以內的不良反應,并將樣本人群分為3個年齡階段:12-15歲、18-55歲、56歲及以上,以研究疫苗對青少年和老年人是否安全。總體來說,第二次接種后絕大多數各類不良反應出現的概率均高于第一次接種后。局部不良反應中,注射處疼痛報告比例較高,第一次、第二次接種后報告疼痛的比例為83.1%、77.8%(對應安慰劑組14.0%、11.7%),其中嚴重疼痛以致于無法進行日常活動的比例為1.0%、1.2%(對應安慰劑組0.1%、0.0%)。系統性不良反應中報告最多的是頭痛和疲憊。在18-55歲主要年齡層的研究中,第一次接種后頭痛和疲憊的出現幾率分別為41.9%、47.4%(對應安慰劑組33.7%、33.4%),第二次接種后的幾率分別為51.7%、59.4%(對應安慰劑組24.1%、22.8%)。其他不良反應中,接種第一劑疫苗后,嘔吐、腹瀉出現的概率分別為1.2%、11.1%,但安慰劑組的對應概率也分別達到1.2%、11.7%,不良反應出現概率與疫苗組持平甚至更高,因此無法判斷此類不良反應的出現是否和疫苗接種有因果關系。相較于第一劑接種,第二劑接種后出現不良反應的概率要更高,出現發熱的頻率達到15.8%(對應安慰劑組0.5%),發冷、肌肉疼痛和關節疼痛的出現頻率也較高,分別為35.1%(對應安慰劑組3.8%)、37.3%(對應安慰劑組8.2%)、21.9%(對應安慰劑組5.2%)。
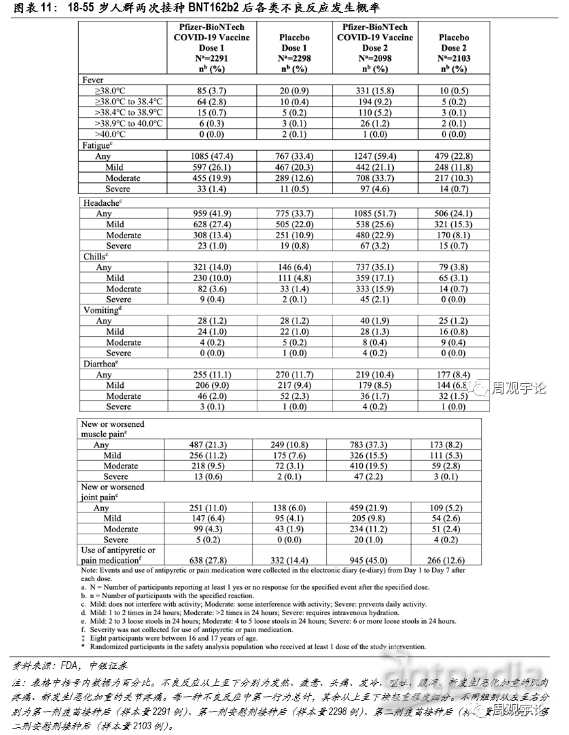
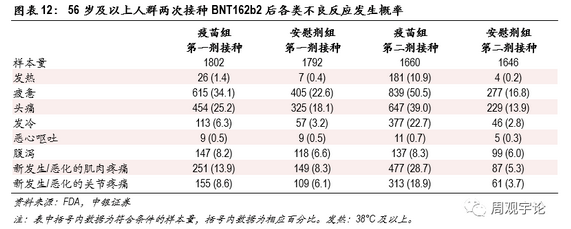
56歲及以上人群接種疫苗后不良反應的發生頻率并未顯示出疫苗會對老年群體造成更嚴重的副作用,老年人群報告的不良反應發生頻率甚至略低于18-55歲年齡段的水平。不同種類的不良反應發生規律與18-55歲年齡層類似,頭疼和疲憊的發生頻率較高。
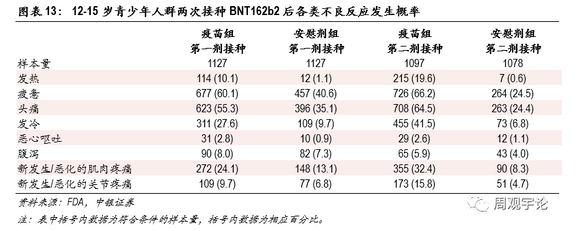
12-15歲年齡層人群接種疫苗后不良反應的發生規律與其他兩個年齡層相似,不良反應發生概率略高于其他兩個年齡層。12-15歲年齡層人群接種疫苗后出現發熱的概率較高。接種第一劑后的發熱概率為10.1%(對應安慰劑組1.1%),接種第二劑后的發熱概率為19.6%(對應安慰劑組0.6%)。
根據CDC數據,截至2021年1月18日,接種BNT162b2疫苗后引起的過敏反應在每百萬人中僅出現5例,概率極低。
(2)Moderna mRNA疫苗(mRNA-1273)安全性
Moderna mRNA-1273的臨床不良反應研究記錄了每劑次接種后7天以內的不良反應,將樣本人群分為2個年齡階段:18-64歲、65歲及以上,同時每個年齡層中分為疫苗組和安慰劑組。總體來說,第二次接種后絕大多數各類不良反應出現的概率均高于第一次接種后。
局部不良反應中,疼痛仍舊是占比最高的,第一次和第二次接種后報告疼痛的比例分別為86.9%、89.9%(對應安慰劑組19.1%、18.7%)。其中三級疼痛報告比例分別為3.2%、4.6%(對應安慰劑組0.2%、0.2%)。
系統性不良反應中,疲憊報告比例仍舊最高,第一次和第二次接種后報告疲憊的比例分別為38.4%、67.6%(對應安慰劑組28.8%、24.6%),與BNT162b2數據相近。
不良反應種類中,除注射處疼痛外,報告最多的不良反應是頭痛和疲憊。在18-55歲主要年齡層的研究中,第一次接種后頭痛和疲憊的出現幾率分別為41.9%、47.4%(對應安慰劑組33.7%、33.4%),第二次接種后的幾率分別為51.7%、59.4%(對應安慰劑組24.1%、22.8%)。其他不良反應中,接種第一劑疫苗后,嘔吐、腹瀉出現的概率分別為1.2%、11.1%,但安慰劑組的對應概率也分別達到1.2%、11.7%,不良反應出現概率與疫苗組持平甚至更高,因此無法判斷此類不良反應的出現是否和疫苗接種有因果關系。相較于第一劑接種,第二劑接種后出現不良反應的概率要更高,出現發熱的頻率達到15.8%(對應安慰劑組0.5%),發冷、肌肉疼痛和關節疼痛的出現頻率也較高,分別為35.1%(對應安慰劑組3.8%)、37.3%(對應安慰劑組8.2%)、21.9%(對應安慰劑組5.2%)。
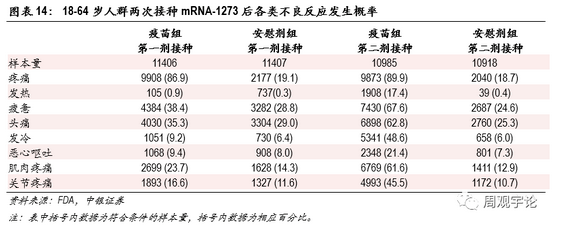
65歲及以上人群接種疫苗后不良反應的發生規律與18-64歲年齡層類似,局部不良反應中疼痛的出現頻率較高,第一次和第二次注射后出現概率分別為74.0%、83.2%(對應安慰劑組12.8%、12.0%)。系統性反應中,頭疼和疲憊的發生頻率較高。第二劑接種后,發熱、發冷、肌肉關節疼痛等不良反應出現概率較第一劑接種后數據上升較為明顯。
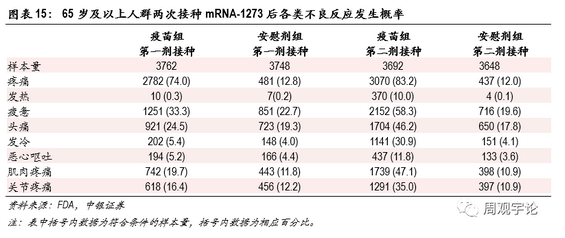
2款mRNA疫苗的III期臨床試驗不良反應數據方面接近,局部反應中疼痛最為普遍,在主要人群中第一劑次和第二劑次平均出現概率為82.4%、85.0%(對應安慰劑組16.3%、15.6%)。系統性不良反應中疲憊與頭痛出現比例較高,在18歲及以上人群接種第二劑次后,疲憊與頭痛的報告比例分別為,三級及以上疲憊的出現概率平均為7.68%(對應安慰劑組0.67%),三級及以上頭痛的出現概率為3.99%(對應安慰劑組0.99%)。
(3)國藥集團滅活疫苗(WIV04/HB02)安全性
傳統疫苗例如滅活疫苗相較而言較為安全,不良反應出現頻率低。滅活疫苗采用的技術路徑相對簡易,外源物質不需要進入細胞(mRNA需要進入細胞質),因此激發的免疫反應較溫和。從臨床數據來看,滅活疫苗這一技術路徑已經過長期不同種類疫苗的驗證,并未發現長期對人體有負面影響。
由于統計標準不同,從國藥集團2款滅活疫苗的III期臨床數據中,我們摘取了第一劑接種后0-28天內(期間部分樣本人群接種了第二劑疫苗)發生的不良反應報告。發生最普遍的仍舊是疼痛,平均發生頻率為21.8%(對應安慰劑組27.9%),顯著低于mRNA疫苗80%左右(對應安慰劑組15%左右)的水平,并且疫苗組數據小于對照組數據。系統性不良反應中,報告頻率較高的是疲憊與頭痛,分別為11.3%、13.4%(對應安慰劑組10.8%、13.0%),其中三級疲憊與頭痛報告比例分別為1.1%、1.0%(對應安慰劑組<0.1%、<0.1%),顯著低于mRNA疫苗數據。
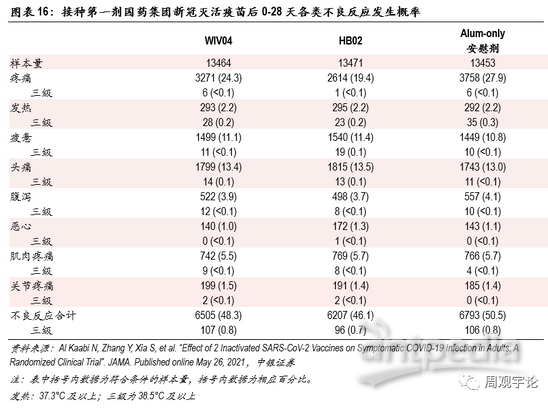
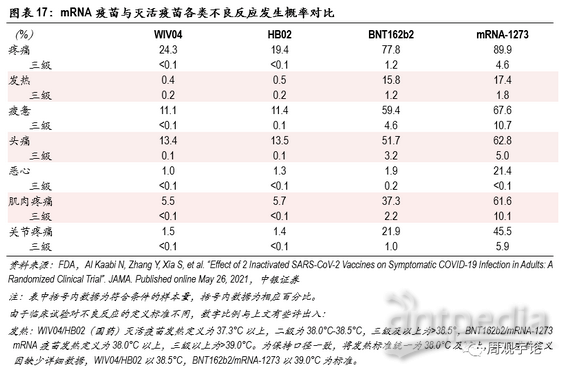
從不良反應發生比例來看,滅活疫苗接種后短期內各項不良反應發生比例明顯低于mRNA疫苗。雖然三款疫苗臨床試驗對于不良反應的定義不同,對照組不同,數據收集周期有差別,但數據上巨大的差異仍能或多或少地體現出mRNA疫苗會帶來較多較強烈的不適。發熱,作為能夠進行橫向量化對比的不良反應之一,在接種mRNA疫苗后出現頻率遠遠高于接種滅活疫苗后的頻率。接種滅活疫苗后發熱(38.0°C以上)的發生比例平均為0.4%,38.5°C以上的發生比例為0.2%;接種mRNA疫苗后發熱(38.0°C以上)的平均發生比例為17.1%,39°C及以上的平均發生比例為1.7%,均高于滅活疫苗的對應數據。
mRNA疫苗臨床數據特點:No pain,no gain
mRNA疫苗同時具有高保護率和相對更多的不良反應。英美俗語“Nopain, no gain” (“沒有痛苦便沒有收獲”),貼切地形容了mRNA疫苗的特點。
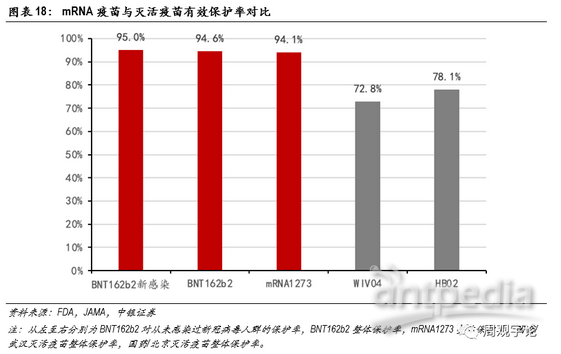
mRNA疫苗對新冠病毒的保護率高達94%以上,國藥傳統滅活疫苗的保護率雖遠遠高于WHO和FDA建議標準的50%,但不足80%,與mRNA疫苗差距明顯。
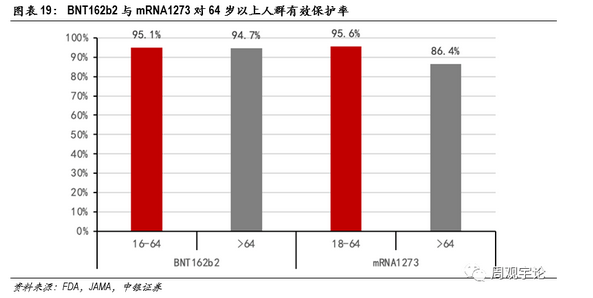
同時,兩款mRNA疫苗均對64歲以上的老年人群展現了非常可觀的保護率。BioNTech的BNT162b2對64歲以上群體的保護率為94.7%,僅比16-64歲群體數據低0.4%。Moderna的mRNA1273對64歲以上人群的保護率也高達86.4%,仍舊高于滅活疫苗的整體數據。
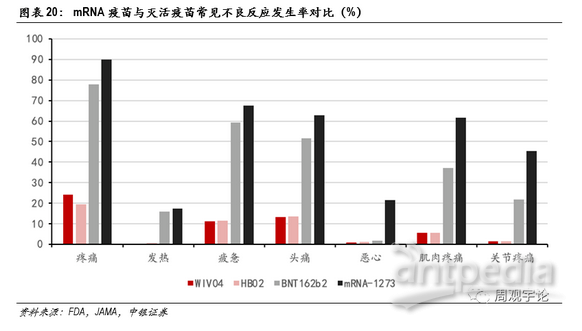
mRNA疫苗嚴重/致命性不良反應罕見但需關注
mRNA疫苗的各項不良反應發生率都較為明顯地高出滅活疫苗對應水平,會讓接種者在短期內產生更多的不適感。但在臨床試驗中并未出現嚴重甚至致命性的不良反應。
各類新冠疫苗在真實世界中開始運用后,不出意外地,開始出現一些此前在實驗階段未曾出現的不良反應,例如血栓伴血小板減少癥候群、心肌炎和心包炎等。
根據美國CDC和FDA數據,截至2021年6月21日,美國共有3款新冠疫苗可供使用,分別為2款mRNA疫苗(輝瑞/BioNTech、Moderna)和1款病毒載體疫苗(強生/楊森)。目前美國共接種3.18億劑次新冠疫苗,其中病毒載體疫苗(強生)接種劑次超1200萬劑次,mRNA疫苗超3億劑次。
綜合3款新冠疫苗的數據,接種后發生過敏的概率為每百萬人中2-5人(概率0.0002%-0.0005%)。
美國疫苗不良反應報告系統(VAERS)目前接到有關心肌炎、心包炎的報告616起(發生概率0.0001%),CDC和FDA已確定其中393
基于病毒的疫苗通常能引發更強的免疫反應,而mRNA疫苗的生產速度更快、成本更低。能否將兩者的優勢結合?一項新研究表明,編碼類似病毒的納米顆粒的mRNA疫苗,而非現有的僅編碼單個蛋白質的新冠mRNA疫苗......
美國耶魯大學研究人員開發出一種新型mRNA疫苗平臺,旨在顯著增強免疫反應、提升mRNA疫苗的有效性,并拓展其在多種疾病預防與治療中的應用潛力。這項發表于最新一期《自然·生物醫學工程》的研究表明,這種疫......
近日,北京立康生命科技有限公司(以下簡稱“立康生命科技”)自主研發的腫瘤新生抗原mRNA疫苗產品——LK101注射液獲得美國食品藥品監督管理局(FDA)的臨床試驗申請(IND)批準。這是我國首個在FD......
合肥阿法納生物科技有限公司研發的呼吸道合胞病毒mRNA疫苗(AFN0205)于2024年7月5日獲得國家藥品監督管理局審評中心核準簽發的《藥物臨床試驗批準通知書》。該品種于2024年4月16日獲得受理......
2024年3月8日,星銳醫藥(StarnaTherapeutics),一家聚焦靶向遞送技術及創新mRNA療法的生物技術公司,宣布其自主研發及生產的呼吸道合胞病毒(RSV)mRNA疫苗STR-V003獲......
即使在新冠疫情期間接種了數十億劑疫苗后,信使核糖核酸(mRNA)疫苗仍令人驚訝。近日,《自然》發表的一項研究表明,mRNA疫苗可能會促使細胞產生少量意想不到的蛋白質。研究人員提出一種解決方案,有助于使......
近日,知乎科技和科學領域的“破曉·2023科技回望”活動引來大量關注。活動以前沿突破為觸角,發布年度“九大科技事件”榜單,在與人們息息相關的科技應用層,展現2023年科學技術領域的“破曉時刻”。202......
9月15日,中國科學院文獻情報中心(簡稱文獻中心)和美國化學文摘社在北京聯合發布《全球mRNA疫苗和治療藥物研究分析報告》。《全球mRNA疫苗和治療藥物研究分析報告》封面。文獻中心供圖《全球mRNA疫......
2019年底突然暴發的新冠疫情讓全世界措手不及,疫情的出現也讓我們看到并見證了mRNA技術的巨大潛力。但目前只有Moderna和輝瑞/BioNTech開發的兩款mRNA疫苗獲批上市。穩定性是mRNA疫......
KNAUER自豪地宣布,他們是今年柏林-勃蘭登堡創新獎的10名主要提名者之一。KNAUER公司因其碰撞噴射混合(IJM)技術而獲得認可,該技術可用于脂質納米顆粒的高流量生產。目前該技術正用于生產mRN......